




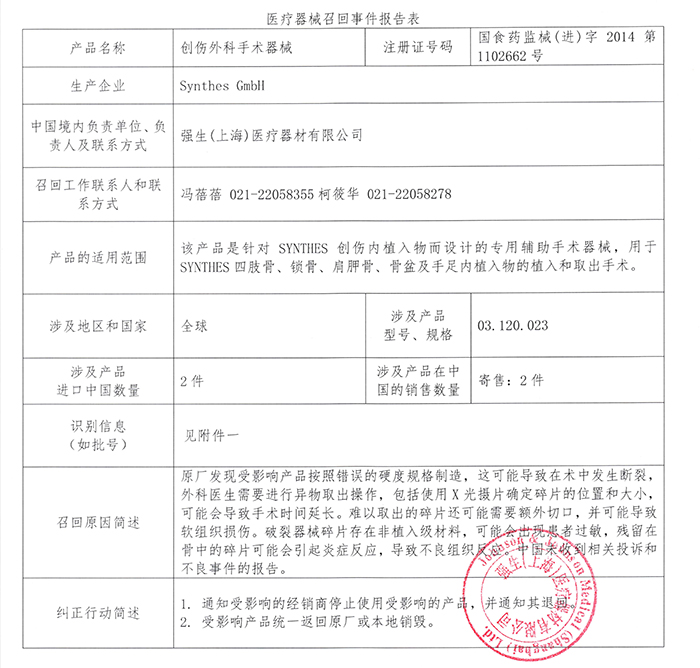
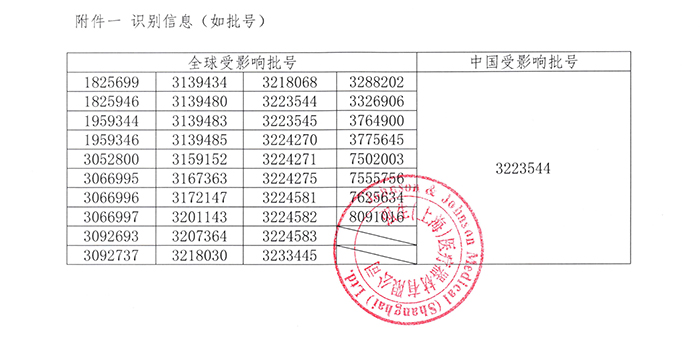
強生(上海)醫(yī)療器材有限公司報告:原廠發(fā)現(xiàn)受影響產(chǎn)品按照錯誤的硬度規(guī)格制造,這可能導(dǎo)致在術(shù)中發(fā)生斷裂,外科醫(yī)生需要進(jìn)行異物取出操作,包括使用X光攝片確定碎片的位置和大小,可能會導(dǎo)致手術(shù)時間延長,難以取出的碎片還可能需要額外切口,并可能導(dǎo)致軟組織損傷,破裂器械碎片存在非植入級材料,可能會出現(xiàn)患者過敏,殘留在骨中的碎片可能會引起炎癥反應(yīng),導(dǎo)致不良組織反應(yīng);中國未收到相關(guān)投訴和不良事件的報告。公司主動召回相關(guān)產(chǎn)品。召回級別為II級。涉及產(chǎn)品的型號、規(guī)格及批次等詳細(xì)信息見《醫(yī)療器械召回事件報告表》。
附件:醫(yī)療器械召回事件報告表
 掃碼進(jìn)入
掃碼進(jìn)入 掃碼進(jìn)入
掃碼進(jìn)入 掃碼打開
掃碼打開 關(guān)注 · 廣州政府網(wǎng)
關(guān)注 · 廣州政府網(wǎng)